V posledních letech bylo dosaženo pokroku v dekódování diagnostických kritérií, která se nadále upřesňují. Mnoho současných hypotéz pro vysvětlení tohoto stavu je však spíše popisem přidružených nálezů, u nichž nebyla jednoznačně stanovena kauzalita. Současná diagnostická kritéria zahrnují regionální bolest, která je nepřiměřená původnímu traumatu, změny barvy a teploty kůže, edém, vazomotorické a sudomotorické změny, motorickou dysfunkci a trofické změny.
Každý model tohoto stavu by měl v ideálním případě vysvětlovat následující skutečnosti:
- Obvykle se KRBS vyvine pouze u 0,5-2 % pacientů s úrazem/traumatem
- Někteří pacienti s KRBS nemají v anamnéze žádné trauma
- U každého pacienta se mohou projevovat jiné příznaky, např. teplá nebo studená končetina, edém, alodynie, hyperalgezie, abnormální pocení a změny na kůži a nehtové tkáni
- CRPS je všeobecně téměř omezen na končetinu (horní nebo dolní) a příznaky (zejména bolest) při chronicitě často postupují proximálně, často až k rameni/boku, ale ne dále.
- Ačkoli se KRBS jeví jako neuropatická bolest, většinou nereaguje na standardní léčbu neuropatické bolesti
- Floridní dystonie může být u části pacientů charakteristickým rysem KRBS a často nereaguje na léčbu
- Periferní příznaky KRBS v chronické fázi onemocnění většinou slábnou a mizí, i když bolest většinou zůstává
V této studii z roku 2018 vychází autoři ze 182 zdrojů a přichází s čtyřsložkovým modelem.
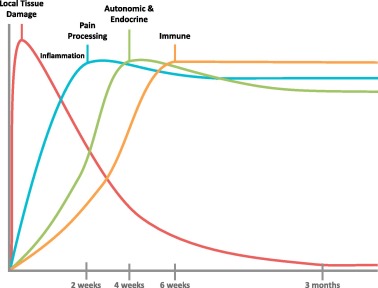
Navrhovaný model KRBS, znázorněný, jako časový průběh homeostatických poruch:
- trauma tkáně (červená linie)
- patologické zpracování bolesti (modrá linie)
- autonomní dysregulace (zelená linie)
- imunitní dysfunkce (oranžová linie)
(U každého jedince se tyto čtyři složky mohou lišit stupněm homeostatické poruchy a relativním časovým průběhem aktivace)
Grafické znázornění celého procesu:
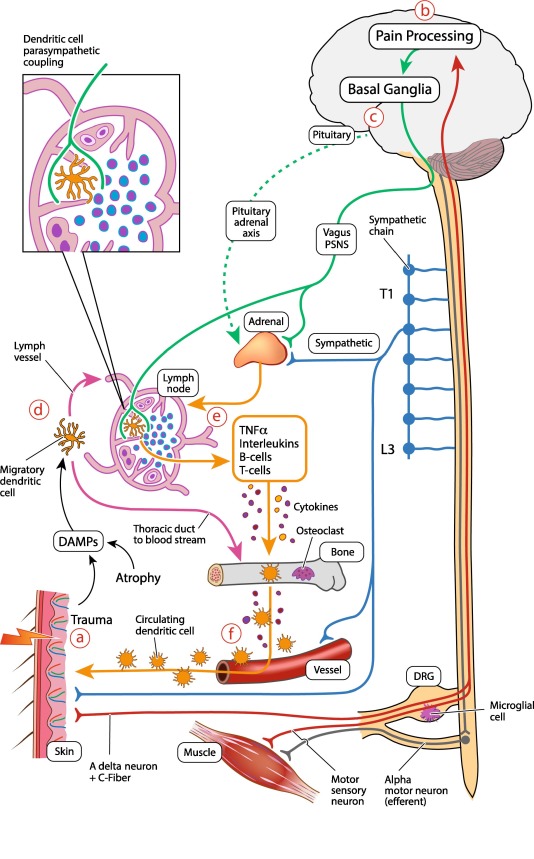
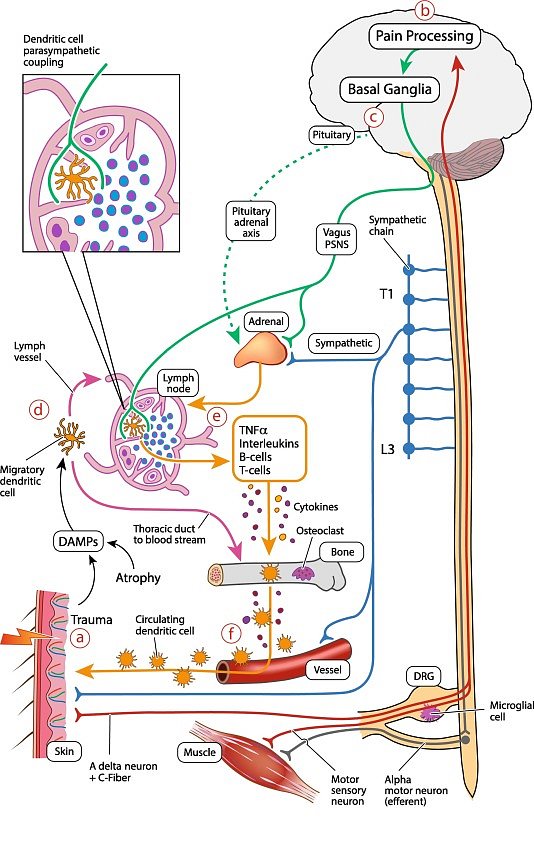
Imunitní odpověď je řízena CNS.
(a) Trauma vede k nocicepci s aktivací mechanických receptorů v místě traumatu. Ta je přenášena aferentními nervovými vlákny (A delta a C vlákna) do DRG (dorsal root ganglion) a do dorzálního rohu míchy segmentálním způsobem. Signály bolesti pak stoupají do mozku, kde se dále zpracovávají.
(b) U KRBS dochází k patologickému zpracování bolesti v kortikálních a subkortikálních oblastech mozku.
(c) Sladění zpracování bolesti s výstupy z bazálních ganglií na autonomní, endokrinní a motorické funkce.
(d) Trauma a atrofie uvolňují DAMPs (damage associated molecular products), které jsou zachycovány dendritickými buňkami, které pak migrují do regionální lymfatické uzliny. Malý počet dendritických buněk projde hrudním kanálem do krevního oběhu.
(e) Za normálních okolností jsou dendritické buňky v lymfatických uzlinách udržovány ve stavu imunitní tolerance inervací autonomního nervového systému, zejména parasympatického nervového systému (PSNS), který moduluje funkci imunitních buněk prostřednictvím cholinergní protizánětlivé dráhy. Autonomní nerovnováha (tj. v důsledku změněné funkce bazálních ganglií a/nebo zvýšeného množství cirkulujících katecholaminů a/nebo sníženého uvolňování parasympatiku (PSNS)/vagového acetylcholinu) vede k přechodu od imunitní tolerance k adaptivní imunitní odpovědi a imunitní kaskádě, při níž se aktivují T-buňky a B-buňky a dendritické buňky a makrofágy uvolňují zánětlivé cytokiny (tj. TNFα, IL-1, IL-18).
(f) Tím je zahájena regionální imunitní odpověď s aktivací osteoklastů a monocytů a expanzí kolonií imunitních buněk, která vede k dalšímu sekundárnímu poškození.
Text v tomto článku slouží spíše jako vodítko k aktuálním informacím pro ty, kteří s lidmi s KRBS pracují. Pro kompletní informace odkazujeme přímo na zmiňovanou studii z roku 2018, kde je vše podrobněji popsáno:
https://www.sciencedirect.com/science/article/pii/S0306987718305668?via%3Dihub#f0025